Entwurf einer Verordnung über klinische Prüfungen (CTT) neuer Techniken und neuer Methoden in der medizinischen Untersuchung und Behandlung, einschließlich Verordnungen zur Zell-Anwendungsforschung, zu den Stufen der CTT von Zellen und Zellprodukten.

Dr. Ngo Quang sagte, dass das Gesundheitsministerium Vorschriften zu TNLS und der Anwendung von Zellprodukten und Zelltherapie erlassen werde.
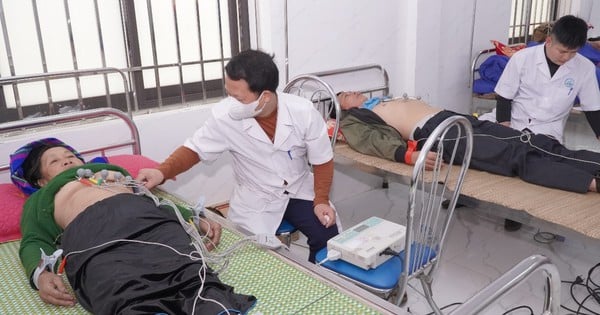
Laut Dr. Ngo Quang wenden viele medizinische Einrichtungen derzeit Zelltherapien an und verstoßen dabei gegen die Vorschriften. Insbesondere werden in der Behandlung und Gesundheitsfürsorge viele Zelltherapiemethoden (Stammzellen, Immunzelltherapie) propagiert, die in Wirklichkeit jedoch wissenschaftlich nicht belegt sind, für die Menschen Folgen haben können oder deren Wirksamkeit unklar ist, was Kosten verursacht.
Die Zelltherapie ist eine neue Methode, eine neue Technik. Vor der Durchführung von Forschungsarbeiten muss diese vom Nationalen Rat für Ethik in der biomedizinischen Forschung geprüft, bewertet und genehmigt werden. Der Forschungsprozess muss eine Bewertung der Sicherheit und Wirksamkeit beinhalten. Nach der Anwendung muss es noch ausgewertet werden, damit die Verwaltungsbehörde entscheiden kann, ob die Umsetzung fortgesetzt oder eingestellt werden soll. Das Endprodukt der Zelltechnologie muss auf Sicherheit und Wirksamkeit kontrolliert werden, um kostspieligen Missbrauch zu vermeiden und zu verhindern, dass die beworbenen Ergebnisse erzielt werden.
Das Gesundheitsministerium vervollständigt derzeit das System der Rechtsdokumente, die die Forschung, klinische Tests und Anwendung von Zelltherapien bei der Behandlung und Gesundheitsfürsorge von Menschen regeln. Die Vorschriften müssen dem Grundsatz der Förderung wissenschaftlicher und technologischer Entwicklung entsprechen, dürfen jedoch nicht spontan erfolgen, und sie müssen sicher und wirksam sein.
[Anzeige_2]
Quellenlink
























































































Kommentar (0)