オーストラリアのRMIT大学のLe Hoang Phuc博士(30歳)と彼の同僚は、薬剤を必要とせずに細菌や真菌から患者を守るために、チタンインプラントに刻まれた微細なスパイクのモデルを作成した。
2020年以来、科学者たちはナノ構造材料上におけるさまざまな有害真菌株間の表面相互作用に関する研究を行っています。新たな研究により、昆虫の羽(セミ、トンボ)にある細菌を殺す棘からヒントを得た微細構造を持つ粗い表面が、真菌などの薬剤耐性スーパーバグと効果的に戦うことが実証された。この研究は9月初旬に『Advanced Materials Interfaces』誌に掲載された。科学者チームはその後、薬剤を必要とせずに細菌や真菌から患者を守るための小さなチタンスパイクのモデルの設計も試みた。

多機能機械抗菌材料研究グループ (左から右へ)、デンバー・リンクレイター、レ・ホアン・フック、エレナ・イワノワ、アルトゥーロ・アブルト・メディナ、カロリン・デ・ソウザ。写真: RMIT大学
チームのアプローチは、接触した微生物を除去することに重点を置いており、それによって化学的な介入を制限する。フック氏は、チームメンバーのデンバー・リンクレイター博士とともに、いくつかの微細なチタンシリンダー表面で実験を行った。
スパイクは細菌細胞の高さと同等の高さになるように特別に設計されています。これらはチタンインプラントの表面に移植され、多剤耐性カンジダを殺す効果についてテストされました。この潜在的に致命的な菌は、病院における医療機器の感染の 10 件中 1 件を占めています。
その結果、小さなチタンスパイクが接触すると、有害な細胞の約半分を破壊することができます。残った真菌細胞は損傷により生存できず、増殖したり感染を引き起こしたりすることはできません。
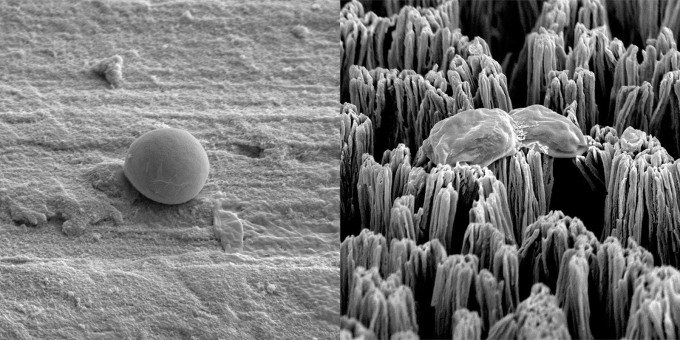
研磨されたチタン表面上の無傷のカンジダ細胞 (左) と、マイクロスパイクチタン表面上の破裂したカンジダ細胞 (右)。写真:研究チーム
デンバー・リンクレイター博士によると、タンパク質代謝分析により、損傷を受けたカンジダ・アルビカンス細胞は最大 7 日間にわたり代謝が広範囲に阻害され、増殖が阻止され、最終的には自滅することが判明しました。残った細胞はもはや生き残ることができず、機能を停止します(アポトーシス、つまりプログラム細胞死と呼ばれます)。
「この発見は、人工抗真菌表面が、危険な多剤耐性酵母によるバイオフィルムの形成をいかに防ぐことができるかを示している」と、昆虫の羽の細菌を殺す能力を最初に研究した研究者の一人であるエレナ・イワノワ教授は述べた。
フック博士は、チタン製マイクロスパイクは実現可能性試験の段階にあると語った。研究チームはまた、このサンプルの抗真菌性をさまざまな微生物株に対してテストし、最適な抗菌および抗バクテリア効果が得られるようにマイクロスパイクのサイズを最適化することを目指しています。
ヌー・クイン
[広告2]
ソースリンク




![[写真] ト・ラム事務総長がベトナム駐在フランス大使オリヴィエ・ブロシェ氏を接見](https://vstatic.vietnam.vn/vietnam/resource/IMAGE/2025/4/17/49224f0f12e84b66a73b17eb251f7278)




















































![[動画] Viettelがベトナム最大の海底光ケーブルラインを正式に運用開始](https://vstatic.vietnam.vn/vietnam/resource/IMAGE/2025/4/17/f19008c6010c4a538cc422cb791ca0a1)






































コメント (0)