Пакистан расследует деятельность двух дистрибьюторов противоракового препарата Авастин компании Roche после того, как 12 пациентов с диабетом, которым делали инъекции этого препарата, ослепли. Авастин также лицензирован во Вьетнаме.
Во Вьетнаме по состоянию на 27 сентября Управление по контролю за лекарственными средствами Вьетнама (Министерство здравоохранения) не получало никаких сообщений, отражающих нежелательные эффекты Авастина, связанные с потерей зрения у пациентов после приема Авастина.
Управление по контролю за лекарственными средствами Вьетнама получило отчет от представительства компании F. Hoffmann La Roche Ltd. по этому вопросу
В частности, в Пакистане около 12 пациентов потеряли зрение после инъекций, предоставленных нелегальным поставщиком Genius Pharmaceutical Service. Препарат имеет маркировку «Инъекции Авастин 1,25 мг/0,05 мл», что создает обманчивое впечатление, что это продукт компании Roche.
Препарат Авастин компании Roche не одобрен для применения при каких-либо офтальмологических показаниях. Компания Genius Pharmaceutical Service осуществила поставку/разбавление/переупаковку препарата в дозировке 1,25 мг/0,5 мл в антисанитарных и несанкционированных условиях.
Пакистанские власти проводят расследование, чтобы определить причину заражения. Причинами могут быть недостаточная стерилизация, загрязненные флаконы, нестерильные шприцы и отклонения от стандартных рабочих процедур при выдаче лекарственных препаратов.
В то же время правительство Пакистана потребовало отозвать три партии препарата Авастин 100 мг/мл (H352B11, B7266B07, B7266B20) компании Roche, а также все препараты, поставляемые компанией Genius Pharmaceutical Service.
(Иллюстрация: 24 News HD).
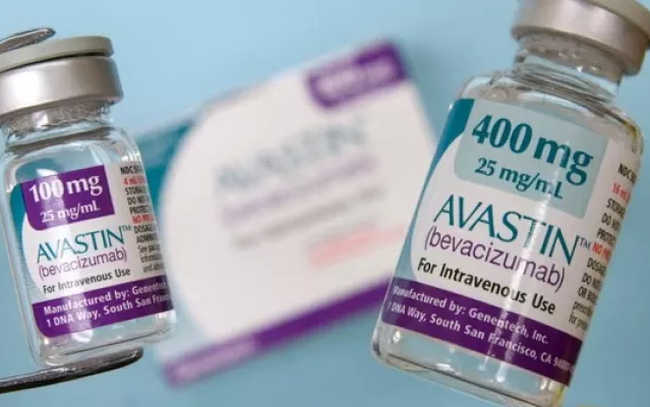
Во Вьетнаме препарату Авастин (действующее вещество Бевацизумаб) выдано 4 свидетельства о регистрации в обращении, все из которых действительны. Включать:
Бевацизумаб 100 мг/4 мл (коробка с 1 флаконом x 4 мл; регистрационный номер: 400410250123 (QLSP-1118-18); производитель: Roche Diagnostics GmbH, Германия).
Бевацизумаб 400 мг/16 мл (коробка с 1 флаконом x 16 мл: регистрационный номер: 400410250223 (QLSP-1119-18); производитель: Roche Diagnostics GmbH, Германия).
Бевацизумаб 100 мг/4 мл (коробка с 1 флаконом x 16 мл; регистрационный номер: QLSP-1010-17; производитель: F. Hoffmann-La Roche Ltd., Швейцария).
Бевацизумаб 400 мг/16 мл (коробка с 1 флаконом x 16 мл; регистрационный номер: QLSP-1011-17; производитель: F. Hoffmann-La Roche Ltd., Швейцария).
Авастин лицензирован для использования во Вьетнаме для лечения некоторых видов рака. Включая метастатический колоректальный рак, распространенный, метастатический или рецидивирующий немелкоклеточный рак легкого, распространенный и/или метастатический почечноклеточный рак, глиобластому/злокачественную глиому (стадия IV по классификации ВОЗ); эпителиальный рак яичников, маточных труб и первичный рак брюшины.
Помимо общих предупреждений, одобренная FDA инструкция по применению препарата включает предупреждение «не для интравитреального применения».
В частности, препарат может вызывать нарушения зрения, а отдельные случаи и группы серьезных нежелательных явлений со стороны глаз были зарегистрированы после интравитреальной инъекции — неодобренного способа введения смесей Авастина из флаконов, предназначенных для внутривенной инфузии у онкологических больных.
К таким реакциям относятся внутриглазная инфекция, эндофтальмит, увеит, отслоение сетчатки, разрыв пигментного эпителия сетчатки, глаукома, внутриглазное кровоизлияние... Некоторые из этих событий приводят к различной степени потери поля зрения, включая постоянную слепоту .
Источник






























































































Комментарий (0)