Lecanemab, cuya marca es Leqembi, es el primer medicamento aprobado en Japón para tratar las causas subyacentes de la enfermedad de Alzheimer y retardar la progresión de los síntomas de la enfermedad.
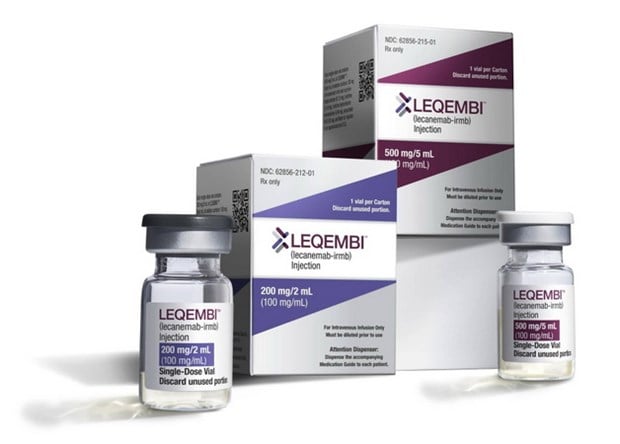
Los viales de Lecanemab, comercializados como Leqembi, están destinados al mercado estadounidense. (Fuente: Kyodo)
Se espera que el medicamento, que trata el deterioro cognitivo leve y en etapa temprana, esté disponible a finales de este año. Sin embargo, los expertos también advierten que este medicamento puede provocar efectos secundarios, incluidos algunos graves.
Anteriormente, un ensayo clínico multinacional mostró que el 17,3% de las personas que tomaron Lecanemab experimentaron sangrado cerebral en comparación con el 9% de los que tomaron placebo, mientras que se observó hinchazón cerebral en el 12,6% con Lecanemab y el 1,7% con placebo.
Los expertos dicen que será necesario monitorear cuidadosamente el estado de las personas tratadas, especialmente si tienen otros problemas de salud.
En Estados Unidos, el medicamento fue aprobado en julio, pero los reguladores han exigido que los pacientes se sometan a pruebas del gen APOE. Las personas con APOE4, uno de los tres tipos de genes APOE, tienen más probabilidades de desarrollar la enfermedad de Alzheimer. APOE4 también es un factor de riesgo para la inflamación y el sangrado cerebral llamado ARIA, causado por medicamentos de anticuerpos. Pero en Japón no se requerirán pruebas genéticas cuando se utilice Lecanemab.
El tratamiento con Lecanemab se administrará en forma de inyección quincenal durante 1,5 años y se controlará el estado del cerebro del paciente mediante exploraciones de resonancia magnética.
Se sabe que el precio de los medicamentos en Estados Unidos es de 26.500 USD al año. También se espera que los precios de los medicamentos en Japón se mantengan altos.
Minh Hoa (reportado por Vietnam+, periódico femenino de la ciudad de Ho Chi Minh)
[anuncio_2]
Fuente


![[Foto] Clausura de la IV Cumbre de la Alianza para el Crecimiento Verde y los Objetivos Globales](https://vstatic.vietnam.vn/vietnam/resource/IMAGE/2025/4/17/c0a0df9852c84e58be0a8b939189c85a)
![[Foto] El Secretario General To Lam recibe al Embajador de Francia en Vietnam, Olivier Brochet](https://vstatic.vietnam.vn/vietnam/resource/IMAGE/2025/4/17/49224f0f12e84b66a73b17eb251f7278)
![[Foto] El periódico Nhan Dan anuncia el proyecto "Ama tanto a Vietnam".](https://vstatic.vietnam.vn/vietnam/resource/IMAGE/2025/4/17/362f882012d3432783fc92fab1b3e980)

![[Foto] Promover la amistad, la solidaridad y la cooperación entre los ejércitos y los pueblos de ambos países.](https://vstatic.vietnam.vn/vietnam/resource/IMAGE/2025/4/17/0c4d087864f14092aed77252590b6bae)
![[Foto] El presidente de la Asamblea Nacional, Tran Thanh Man, se reúne con destacados trabajadores de la industria del petróleo y el gas.](https://vstatic.vietnam.vn/vietnam/resource/IMAGE/2025/4/17/1d0de4026b75434ab34279624db7ee4a)






















![[Foto] Ceremonia de bienvenida al Ministro de Defensa chino y a la delegación para el intercambio de amistad.](https://vstatic.vietnam.vn/vietnam/resource/IMAGE/2025/4/17/fadd533046594e5cacbb28de4c4d5655)



























![[Vídeo] Viettel pone oficialmente en funcionamiento la línea de cable óptico submarino más grande de Vietnam](https://vstatic.vietnam.vn/vietnam/resource/IMAGE/2025/4/17/f19008c6010c4a538cc422cb791ca0a1)





































Kommentar (0)