Агентство также заявило, что обновленная вакцина, разработанная компаниями Pfizer-BioNTech и Moderna, станет новой основной вакциной против COVID-19 и отменит разрешение на экстренное использование старых вакцин, которые нацелены только на исходные варианты коронавируса.
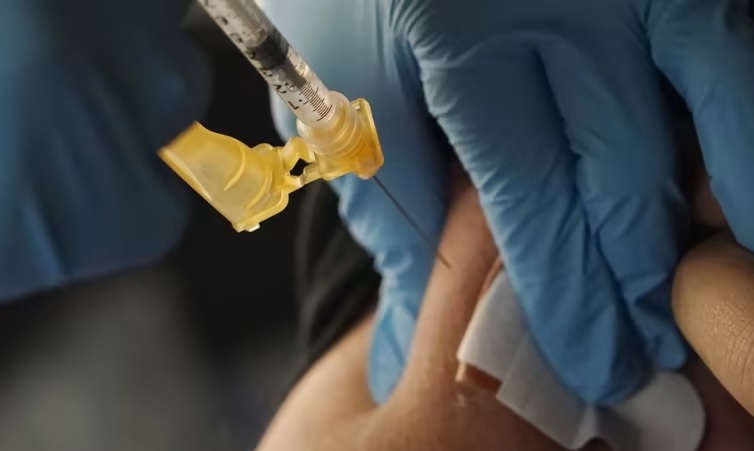
Фото: АП
Агентство сообщило, что люди в возрасте 65 лет и старше теперь могут получить вторую ревакцинирующую дозу новой вакцины через четыре месяца после первой прививки, в то время как лица с иммунодефицитом могут получить дополнительную дозу обновленной вакцины через два месяца.
Решение FDA было принято за день до заседания экспертно-консультативной группы Центров США по контролю и профилактике заболеваний (CDC) по обновлению рекомендаций по вакцинации от COVID-19.
Центрам по контролю и профилактике заболеваний придется выпустить эти вторые прививки, специально разработанные для Omicron, чтобы они стали широкодоступными. FDA одобрило эту новую вакцину против COVID-19 в августе прошлого года, нацеленную на подварианты Omicron BA.4 и BA.5, а также на исходный штамм COVID.
Лишь около 17% населения США получили две дозы этой вакцины с химиотерапией, однако среди людей в возрасте 65 лет и старше уровень вакцинации выше — около 42,6%.
Отзыв разрешения на старые вакцины от Moderna и Pfizer-BioNTech произошел в то время, когда FDA планирует перейти к кампании, аналогичной той, которую американцы получают от прививок от гриппа.
FDA также заявило, что проведет еще одну встречу со своими консультантами в июне, чтобы обсудить вакцины от COVID-19 на следующую осень, при этом ожидается, что производители вакцин на основе мРНК обновят свои вакцины после того, как будут выбраны конкретные штаммы.
Хоанг Ань (по данным Reuters, CNA, AP)
Источник



![[Фото] Укрепление дружбы, солидарности и сотрудничества между армиями и народами двух стран](https://vstatic.vietnam.vn/vietnam/resource/IMAGE/2025/4/17/0c4d087864f14092aed77252590b6bae)
![[Фото] Газета Nhan Dan анонсирует проект «Люблю Вьетнам так сильно»](https://vstatic.vietnam.vn/vietnam/resource/IMAGE/2025/4/17/362f882012d3432783fc92fab1b3e980)
![[Фото] Закрытие 4-го саммита Партнерства ради зеленого роста и глобальных целей](https://vstatic.vietnam.vn/vietnam/resource/IMAGE/2025/4/17/c0a0df9852c84e58be0a8b939189c85a)
![[Фото] Председатель Национальной ассамблеи Чан Тхань Ман встречается с выдающимися работниками нефтегазовой отрасли](https://vstatic.vietnam.vn/vietnam/resource/IMAGE/2025/4/17/1d0de4026b75434ab34279624db7ee4a)
![[Фото] Генеральный секретарь То Лам принимает посла Франции во Вьетнаме Оливье Броше](https://vstatic.vietnam.vn/vietnam/resource/IMAGE/2025/4/17/49224f0f12e84b66a73b17eb251f7278)
















![[Фото] Церемония приветствия министра обороны Китая и делегации для дружеского обмена](https://vstatic.vietnam.vn/vietnam/resource/IMAGE/2025/4/17/fadd533046594e5cacbb28de4c4d5655)




























![[Видео] Viettel официально вводит в эксплуатацию крупнейшую подводную оптоволоконную кабельную линию во Вьетнаме](https://vstatic.vietnam.vn/vietnam/resource/IMAGE/2025/4/17/f19008c6010c4a538cc422cb791ca0a1)





































Комментарий (0)