SGGPO
주사용 페노바르비탈 21,000병이 오랜 중단 끝에 베트남에 도착하여 호치민시의 심각한 손발구병 치료를 위한 중요한 의약품 공급원을 즉시 보충했습니다.
 |
8월 9일, 호치민시 보건부는 페노바르비탈 주사액 21,000개가 오랜 중단 끝에 베트남에 도착했다고 발표했습니다. 이는 호치민시의 3개 소아 전문 병원과 열대병 병원에서 심각한 손발구병(HFMD) 치료를 위한 약물 공급을 신속하게 보완하는 것입니다. 이전에 호치민시 보건부는 TCM 질병 치료를 위해 감마글로불린 1,000병을 받았습니다.
호치민시 보건부에 따르면, 2020년 말 현재 페노바르비탈의 국내 공급이 제한되어 장기간 중단되었습니다. 보건복지부 전문가 협의회는 회의를 열고 현재 시중에 판매되고 있는 디아제팜, 미다졸람 등의 다른 일시적 진정제를 대체할 약을 선택하기로 합의했으며, 베트남 제약 회사들이 다른 국가에서 공급원을 찾을 때까지 기다릴 예정이다. 동시에 보건부는 베트남 약품관리국과 보건부에 페노바르비탈에 대한 병원의 치료 수요를 충족시키기 위해 약물 공급원을 찾고 회사를 수입하도록 지원해 줄 것을 요청하는 공식 공문을 보냈습니다.
6월 22일, 베트남 약품관리국은 제조업체인 대신약품(주)이 더 이상 다노탄을 생산하지 않을 것이라고 답변했습니다. 행정부는 약물 수입 회사에 외국 파트너와 연락하여 대체 약물 공급원을 찾도록 요청하는 문서를 보냈습니다.
2023년 2월 1일까지 Central Pharmaceutical Joint Stock Company CPC1은 페노바르비탈의 대체 공급업체를 찾았고 베트남 약품 관리국으로부터 제조업체인 Incepta Pharmaceutical Ltd(방글라데시)에서 베트남으로 200mg/ml의 바르빗 주사액(페노바르비탈 주사액) 21,000병을 수입할 수 있는 허가를 받았습니다.
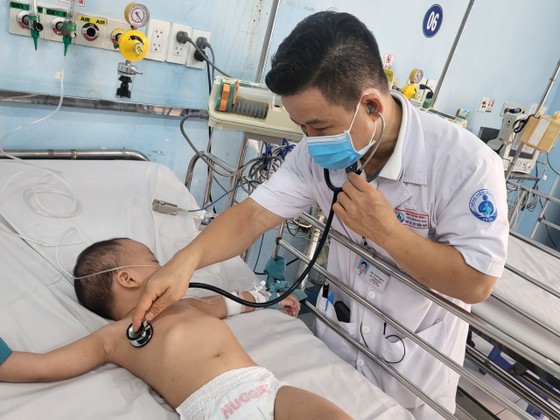 |
1소아병원의 의사들이 심각한 손발구병을 앓고 있는 어린이를 진찰하고 있습니다. |
7월 31일까지, 페노바르비탈은 특별 관리가 필요한 약물 그룹에 속하는 향정신성 약물이기 때문에 수출국의 유관 기관에서 수출 허가를 받아야 하기 때문에 장기간의 서류 작업 끝에 21,000개의 주사용 페노바르비탈 튜브가 베트남에 도착했고, 중앙제약 주식회사 CPC1에서 즉시 이를 소아 전문 병원과 호치민시 열대병원에 공급하여 전염병이 가장 극심했던 시기에 중의학 질병을 치료하는 데 활용했습니다.
페노바르비탈은 보건부가 2012년 3월 30일자 제1003/QD-BYT호 결정을 통해 발표한 TCM 치료 요법에 포함된 중요한 치료제입니다. 이 요법에 따르면, 페노바르비탈은 경구 또는 주사로 사용할 수 있으며, 심각한 경우에는 주사가 선호됩니다. 페노바르비탈은 많은 이점이 있고 부작용이 거의 없어 어린이에게 사용되며, 오랫동안 소아 환자에게 의사들이 사용해 왔습니다.
중의학에서 페노바르비탈은 장기 발작을 멈추고 발작 재발을 예방하는 데 역할을 합니다. 또한 이 약은 진정 효과가 있어 어린이의 신경 증상과 놀람을 줄이는 데 도움이 됩니다. 또한 뇌부종이 있는 경우(심각한 경우) 이 약물은 뇌부종을 감소시키고 뇌의 산소 소비 필요량을 줄이는 데 도움이 됩니다.
주사용 페노바르비탈은 작용이 빠르게 나타나고(주사 후 5분), 효과가 최고조에 달하는 시간도 빠르게(15~30분) 나타나며, 작용 지속 시간도 비교적 짧습니다(6시간). 경구형에 비해 작용 시작이 늦고(60분 이상), 작용 지속 시간이 길며(10~12시간) 각 어린이의 흡수에 따라 주사용 페노바르비탈은 위험군과 중증군(2b군, 3군)의 TCM을 앓고 있는 어린이에게 적합합니다.
호치민시 보건부의 통계에 따르면, 2023년 초부터 현재까지 호치민시에서는 15,753건 이상의 중의학 감염 사례가 발생했습니다. 매일 수백 건의 신규 확진자가 발생하고, 다른 지역에서 옮겨온 심각한 사례도 많습니다. 이 중 병원에 입원한 환자는 대부분 6세 미만의 어린이입니다.
국내 자원을 적극적으로 공급하기 위해, 미국 식품의약국(FDA)은 주사용 페노바르비탈을 생산하기 위해 다나파 제약 주식회사에 페노바르비탈 원료를 수입할 수 있는 허가를 부여했습니다. 회사는 생산 계획을 실행하고 있습니다.
[광고_2]
원천




![[사진] 토람 사무총장, 러시아 공식 방문 시작, 파시즘 전승 80주년 기념 행사 참석](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/8/5d2566d7f67d4a1e9b88bc677831ec9d)
![[사진] 국회의장 쩐탄만, 제1차 국회당대회 문서분과위원회 회의 주재](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/8/72b19a73d94a4affab411fd8c87f4f8d)
![[사진] 팜민친 총리, 민간경제개발정책자문위원회와 회동](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/8/387da60b85cc489ab2aed8442fc3b14a)
![[사진] 루옹 꾸엉 대통령이 대통령실 부실장 임명 결정 발표](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/8/501f8ee192f3476ab9f7579c57b423ad)





























































































댓글 (0)