Actuellement, les essais cliniques au Vietnam sont principalement des essais servant au développement de nouveaux produits tels que : médicaments, vaccins, équipements médicaux , nouvelles techniques de traitement... En particulier, ces dernières années, des études ont été menées sur la thérapie cellulaire et génique.
Les essais cliniques doivent être approuvés et évalués de près avant leur mise en œuvre, car le processus de test, les nouveaux produits et les nouvelles techniques peuvent présenter des risques pour les volontaires participant à la recherche.
Cependant, en réalité, au fil des années, des études ont été approuvées par des ministères et des secteurs autres que le ministère de la Santé pour mener des recherches sur des êtres humains, mais non approuvées par le Conseil d’éthique de la recherche biomédicale.
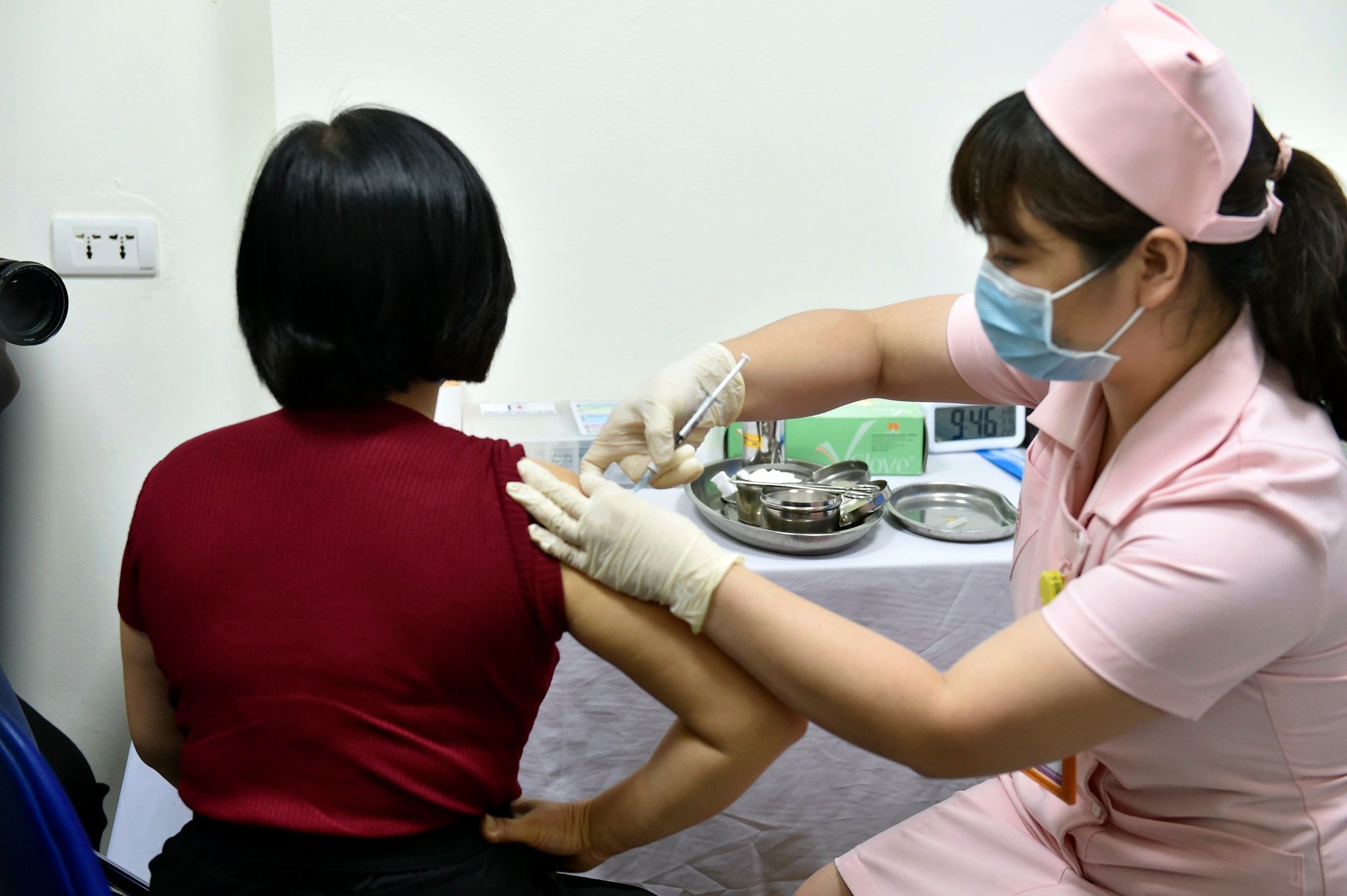
Injection expérimentale du vaccin Covivac contre la Covid-19 à l'Université de médecine de Hanoi , mars 2021
Le ministère de la Santé sollicite des commentaires sur un projet de circulaire réglementant la gestion des tâches scientifiques et technologiques sous la responsabilité du ministère de la Santé. Le projet propose que les sujets de recherche financés par des sources non budgétaires, gérés par d’autres ministères et secteurs mais impliquant des recherches humaines, ne puissent être menés qu’après l’approbation du Conseil d’éthique de la recherche biomédicale et la ratification du ministère de la Santé. Dans le même temps, le projet souligne et promeut également le rôle des conseils de base au niveau des unités dans l’approbation des grandes lignes de recherche, la réduction du temps d’approbation au ministère de la Santé et la garantie des progrès de la recherche.
Au Vietnam, il y a environ 100 essais cliniques chaque année, ce qui est un facteur favorable pour que le pays accède à de nouvelles technologies, produits et méthodes de traitement et de soins de santé, en particulier pour les maladies difficiles telles que le cancer, les maladies cardiovasculaires, etc. Lorsque de nouveaux produits et techniques sont approuvés, le Vietnam sera également le lieu où ils pourront y accéder rapidement, y compris les médicaments, les vaccins, etc. Cependant, avant d'être officiellement autorisé, le processus d'essai clinique peut présenter des risques pour la santé et la vie des volontaires, il est donc nécessaire d'être strictement approuvé et surveillé pendant la mise en œuvre.
Conformément à la réglementation en vigueur, le ministère de la Santé est chargé de gérer, d’orienter et d’organiser la mise en œuvre de la recherche biomédicale sur des sujets humains. Pour les tâches scientifiques et technologiques liées à la recherche biomédicale sur des sujets humains, avant d'exécuter la tâche, l'organisme en charge de la tâche doit avoir l'approbation du Conseil d'éthique de la recherche biomédicale (comme prescrit dans la circulaire n° 04/2020/TT-BYT).
Lien source


![[Photo] Les dirigeants du Parti et de l'État assistent au programme artistique spécial « Vous êtes Ho Chi Minh »](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/18/6895913f94fd4c51aa4564ab14c3f250)

![[Photo] Prêt pour les plus grandes compétitions de tennis de table vietnamien](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/18/9c547c497c5a4ade8f98c8e7d44f5a41)

![[Photo] De nombreux jeunes ont patiemment fait la queue sous le soleil brûlant pour recevoir un supplément spécial du journal Nhan Dan.](https://vphoto.vietnam.vn/thumb/1200x675/vietnam/resource/IMAGE/2025/5/18/6f19d322f9364f0ebb6fbfe9377842d3)





























































































Comment (0)